Testarea genetică pozitivă în cancerul de sân: semnificație și atitudine
Testarea genetică pozitivă în cancerul de sân: semnificație și atitudine
Testarea genetică pozitivă în cancerul de sân: semnificație și atitudine
La ora actuală, este o certitudine că prezența mutațiilor genelor BRCA 1, BRCA 2 și PALB 2 crește semnificativ riscul dezvoltării unui cancer mamar de-a lungul vieții.
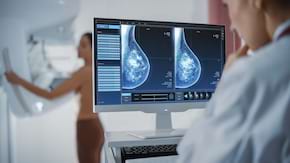
Testarea genetică pentru cancerul mamar și ovarian
Testarea genetică pentru cancerul mamar și ovarian ereditar dezvăluie informații semnificative privind riscul, și are implicații potențiale atât pentru pacienți, cât și pentru familiile acestora. În Regatul Unit, testarea genetică este oferită numai persoanelor cu un istoric familial puternic de cancer, la care există cel puțin 20% șanse de a găsi o mutație genetică predispozantă la cancer. Pentru ca o persoană neafectată să fie eligibilă pentru un test genetic pentru predispoziția la cancer, trebuie mai întâi să fie identificată o mutație patogenă la o rudă cu cancer.
La consilierea genetică, se sugerează că persoanele depistate ca fiind purtătoare a unei mutații BRCA 1 sau BRCA 2 ar putea dori să informeze rudele cu privire la rezultat și la disponibilitatea testării genetice de screening și predictive, având astfel un rol central în facilitarea luării unei decizii în cunoștință de cauză și a opțiunilor de gestionare a riscului pentru ceilalți. Astfel, statutul genetic al unui individ are implicații biologice, psihologice și relaționale pentru membrii familiei.
Literatura de specialitate existentă privind motivațiile și procesul decizional în materie de testare genetică este în mare parte explorată în mod izolat de contextul familial și fără a lua în considerare influența pe care comunicarea și relațiile familiale o pot avea asupra indivizilor. Cercetările sugerează că comunicarea familială a informațiilor privind riscul genetic este foarte selectivă, atât în ceea ce privește ceea ce se spune, cât și cui, ceea ce poate influența deciziile rudelor de a solicita tratament sau screening. Se știe că procesele familiale sunt o parte inerentă a procesului decizional individual, iar testarea la un membru al familiei poate influența procesul decizional și motivațiile unui alt membru al familiei.
Mutațiile genetice
Dacă riscul unui cancer mamar sporadic, de-a lungul vieții, este estimat la aproximativ 12%, femeile care "poartă" în ADN-ul lor mutațiile genelor BRCA 1 și BRCA 2 (cele mai cunoscute și caracterizate, în acest moment) prezintă un risc de cancer mamar cuprins între 40 și 85%, ceea ce înseamnă de 3-7 ori mai mare.
De asemenea, dacă pentru cancerul ovarian riscul apariției în populație este de aproximativ 2%, mutația genelor BRCA 1 și BRCA 2 crește acest risc la un procent cuprins între 15 și 45%. Bărbații purtători ai mutațiilor BRCA și, în special BRCA 2, prezintă un risc estimat de peste 7 ori de apariție a unui cancer mamar. În plus, riscul este crescut pentru apariția unui cancer prostatic.
În afara genelor BRCA 1 și BRCA 2, arhicunoscute în testarea predictivă în acest moment, bateriile de testare includ din ce în ce mai frecvent și mutațiile genei PALB 2, frecvent asociată riscului de apariție a cancerului mamar (risc estimat de 30-60%). Cercetările în privința acestei gene sunt în derulare și urmăresc cuantificarea riscului de cancer mamar și ovarian, dar și de cancer mamar sau pancreas la bărbații purtători ai acestei mutații.
Identificarea mutațiilor genelor BRCA 1, BRCA 2 sau PALB la subiecți sănătoși înseamnă o probabilitate de 50% de transmitere către descendenți. Cu totul excepțional, anumite persoane pot prezenta o mutație atât a genei BRCA 1, cât și a genei BRCA2. În general, aceste persoane sunt componente ale grupului etnic de evrei askhenazi.
În ceea ce privește atitudinea de screening și de monitorizare, aceasta este similară purtătorilor mutațiilor unigenă.
Femeile cu mutații BRCA 1 sau BRCA 2 diagnosticate cu un cancer mamar nu prezintă un risc suplimentar de dezvoltare a cancerelor mamare multiple în sânul afectat.
În ceea ce privește caracteristicile cancerului mamar dezvoltat în condițiile mutațiilor genei BRCA 1, acesta este preponderent cu receptori hormonali negativi, este înalt agresiv și principala atitudine terapeutică este reprezentată de chimioterapie. De asemenea, aceste tumori, inclusiv cele care exprimă gena BRCA 2, nu exprimă gena HER 2.
Prin urmare, marea majoritate a tumorilor care exprimă gene defective BRCA 1 sau BRCA 2 sunt triplu negative, entitate care nu exprimă nici receptori hormonali și nici gena HER 2. Aceste tumori sunt recunoscute ca tumori agresive, cu potențial foarte mare de recidivă sau de metastazare.
Atitudinea în cazul unei mutații BRCA moștenite este variată și depinde, între altele, și de opțiunea pacientei. Consultul genetic cuantifică riscul de a dezvolta un cancer mamar și ovarian și, în funcție de aceasta, se comunică pacientei variantele de management al cazului care pot varia de la screeningul mamar intensiv, chemoprevenție, până la mastectomia bilaterală profilactică și/ sau ovarectomia profilactică.
În ceea ce privește ovarectomia profilactică, alegerea momentului optim depinde de mutația genetică identificată, BRCA 1 sau BRCA 2. Pentru mutațiile BRCA 1, vârsta optimă recomandată pentru efectuarea intervenției de îndepărtare a ovarelor și a trompelor este cuprinsă între 35 și 40 de ani. Pentru purtătoarele mutațiilor genei BRCA 2, vârsta optimă recomandată pentru ovarectomie este cuprinsă între 40 și 45 de ani.
Terapia profilactică cu modulatori selectivi ai receptorilor de estrogen (Tamoxifen, Raloxifen) sau cu inhibitori de aromatază (Anastrozol, Exemestan, etc.) s-a dovedit eficientă în scăderea riscului de dezvoltare a cancerelor mamare cu receptorii pozitivi, dar nu și în ce privește dezvoltarea cancerelor mamare fără receptori hormonali.
Screeningul mamar intensiv înseamnă examinare clinică semestrială, autoexaminare lunară, RMN mamar anual, începând cu vârsta de 25 de ani, sau mamografie, acolo unde examinarea RMN nu este disponibilă. În cazul în care un membru al familiei este diagnosticat cu cancer mamar la vârsta de 30 de ani, screeningul trebuie să înceapă chiar mai devreme de 25 de ani. Examinarea clinică la bărbații cu mutații BRCA 1 sau BRCA 2 trebuie să înceapă la 35 de ani.
În privința screeningului cancerului ovarian, aceasta trebuie să înceapă între 30 și 35 de ani și constă în ecografie transvaginală și monitorizarea anuală a markerului CA125.
Atitudinea în cazul unei paciente deja diagnosticate cu cancer mamar
În condițiile în care o pacientă este diagnosticată cu cancer mamar și prezintă o mutație BRCA sau PALB, atitudinea terapeutică poate fi nuanțată. În general, pacientele cu cancer mamar și mutație BRCA 1 sunt preponderent estrogen negative și, prin urmare, candidate pentru chimioterapie, în timp ce purtătoarele de mutație BRCA 2 sau PALB sunt mai degrabă estrogen pozitive și, prin urmare, hormonoterapia este opțiunea terapeutică pentru acestea.
Femeile diagnosticate cu cancer mamar și cele care prezintă mutații BRCA 1 sau BRCA 2 prezintă un risc semnificativ crescut de a dezvolta un nou cancer mamar primitiv, dar și un cancer ovarian, iar abordarea va fi punctuală și se va discuta cu medicul curant, alegând între supraveghere activă, terapie preventivă sau intervenție chirurgicală ablativă în scop profilactic.
Nu uitați că un diagnostic corect poate fi pus doar de către un medic specialist, în urma unui consult și a investigațiilor adecvate. Puteți face chiar acum o programare, prin platforma DOC-Time, aici. Iar dacă nu sunteți siguri la ce specialist ar fi indicat să mergeți, vă recomandăm să începeți cu un consult de medicină internă, pentru care puteți face, de asemenea, programări prin DOC-Time.
Sursă foto: Shutterstock
Bibliografie:
Breast Cancer - What to Do if Your Genetic Test Results Are Positive - https://www.breastcancer.org/symptoms/testing/genetic/pos_results
Te-ar mai putea interesa și...